Закон збереження маси речовин, відкритий М. В. Ломоносовим в 1756 р говорить:
Маса речовин, що вступили в реакцію, дорівнює масі речовин, що вийшли в результаті її.
Матеріальними носіями маси речовин є атоми хімічних елементів, з яких складаються як вступили в реакцію речовини (реагенти), так і утворилися в результаті її нові речовини (продукти реакції). Оскільки при хімічних реакціях атоми не утворюються н не руйнуються, а відбувається лише їх перегрупування, то стає очевидним справедливість відкритого М. В. Ломоносовим і підтвердженого пізніше А. Лавуазьє закону.
У справедливості закону збереження маси речовин можна легко переконатися на простому досвіді. Помістимо в колбу трохи червоного фосфору, закриємо її корком і зважимо на терезах. Потім колбу, обережно нагріємо.
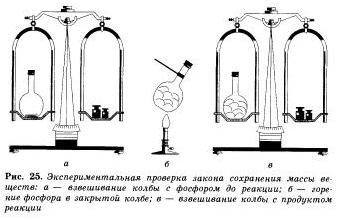
Про те, що сталася хімічна реакція. нам стане зрозуміло по появі густого білого диму в колбі, що складається з оксиду фосфору (V). який утворився при взаємодії фосфору з киснем. При повторному зважуванні колби з продуктами цієї реакції ми переконаємося, що маса речовин в колбі не змінилася, хоча і відбулося перетворення фосфору в його оксид.
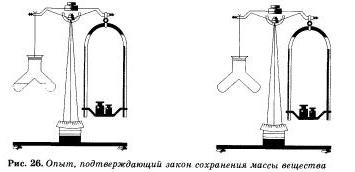
Цей же висновок буде нами зроблений і при проведенні ще одного простого, але дуже наочного досвіду. В спеціальну посудину наллємо окремо соляну кислоту і розчин лугу, наприклад гідрокспда натрію. До розчину лугу додамо кілька крапель індикатора - фенолфталеїну, чому розчин забарвиться в малиновий колір. Закриємо прилад пробкою, врівноважити гирями на вагах, відзначимо масу, а потім злити розчини. Малинова забарвлення зникне, тому що кислота і луг прореагував і один з одним. Маса ж судини з отриманими продуктами реакції не змінилася.
На підставі цього закону пишуться хімічні пропозиції, тобто складаються рівняння хімічних реакцій за допомогою хімічних слів - формул.
Хімічні рівнянням називається умовний запис хімічної реакції за допомогою хімічних формул і математичних знаків.
У лівій честі рівняння записують формули (формулу) речовин, що вступили в реакцію, з'єднують їх знаком плюс. У правій частині рівняння записують формули (формулу) утворюються речовин, також з'єднаних знаком плюс. Між частинами рівняння ставлять стрілку. Потім знаходять коефіцієнти - числа, які стоять перед формулами речовин, щоб число атомів однакових елементів в лівій і правій частинах рівняння були рівні.
Запишемо, наприклад, таке рівняння реакції:
Так як число атомів кисню в першій частині вдвічі більше, ніж в лівій, запишемо перед формулою води коефіцієнт 2:
2Н2О -> Н2 + О2
Але тепер в лівій дріботячи рівняння стало чотири атома водню, а в правій їх залишилося два. Щоб зрівняти число атомів водню, запишемо перед його формулою в правій частині також коефіцієнт 2. Так як ми зрівняли число атомів кожного елемента в лівій і правій частинах рівняння, замінимо стрілку на знак рівності:
2H2O = 2Н2 + О2
Тепер, напевно, вам зрозуміло, чому такий запис називається рівнянням.
За допомогою рівнянь хімічних реакцій можна визначити і тип реакції. Так, розглянута вище реакція відноситься до реакція я розкладання, тобто таким, при яких мул одного складного речовини утворюються два і більше нових простих або складних речовини, але більш простого складу.
При розкладанні, наприклад, гідроксиду заліза (III) утворюються оксид заліза (III) і вода:
Хімічні реакції протилежного типу називаються реакціями з'єднання. В реакції з'єднання вступають одне або кілька простих або складних речовин, з яких утворюється одне більш складна речовина.
Наприклад, водень і кисень при горінні, з'єднуючись, утворюють воду:
До реакцій з'єднання відноситься і розглянута раніше нами реакція отримання сульфіду заліза (II) з порошків сірки і заліза. Цікаво відзначити, що реакції з'єднання і реакції розкладання супроводжуються протилежними тепловими ефектами: реакції з'єднання частіше ставляться до екзотермічним. а реакції розкладання - до ендотермічним.
Якщо в розчин сульфату міді (ІІ) опустити залізну скріпку, то дуже скоро вона почервоніє через виділилася на ній міді, а в розчин перейде сульфат заліза (II):
CuSO4 + Fe = FeSO4 + Cu
Ми записали рівняння реакції заміщення, тобто такої реакції, при здійсненні якої атоми простої речовини заміщають атоми одного нє елементів а складному речовині.
В результаті цієї реакції утворюються два нових речовини - просте і складне.
До реакція обміну відносяться такі реакції, при яких два складних речовини обмінюються своїми складовими частинами.
Наприклад, до розчину мідного купоросу сульфату міді (II) Доллємо кілька крапель розчину едкою натру - гідроксиду натрію, випадає блакитний осад гідроксиду міді (II). При цьому утворюється ще одне складне речовина - розчинна сіль сульфат натрію:
Якщо до отриманого осаду долити розчин сірчаної кислоти, то ми помітимо розчинення отриманого осаду в результаті іншої реакції обміну:
Cu (OH) 2 + H2SO4 = CuSO4 + 2HOH
Отже, рівняння хімічної реакції показує, які речовини вступають у взаємодію і які речовини при цьому утворюються, в яких кількісних відносинах вони знаходяться і якого типу ця реакція.
Наприклад, рівняння
4Al + 3O2 = 2Al2O3
показує, що в результаті реакції з'єднання чотири благаючи алюмінію взаємодіють з трьома молями кисню і утворюють при цьому два благаючи оксиду алюмінію.
1. Хімічні рівняння.
2. Реакції розкладання.
3. Реакції з'єднання.
4. Реакції заміщення.
5. Реакції обміну.
Запишіть у вигляді хімічних рівнянь наступні пропозиції: а) При випалюванні карбонату кальцію утворюються оксид кальцію і оксид вуглецю (IV)
б) При взаємодії оксиду фосфору (V) з водою виходить фосфорна кислота. Який тип зазначених реакцій? Яка з них буде екзо-, а яка ендотермічної?
Складіть рівняння за такими схемами і вкажіть тип реакції:
Під формулами речовин напишіть їх назви. Запишіть рівняння хімічних реакцій за такими схемами:
а) фосфорна кислота + гідроксид натрію -> фосфат натрію + вода;
б) оксид натрію + вода -> гідроксид натрію;
в) оксид заліза (II) + алюміній -> оксид алюміній + залізо;
г) гідроксид міді (II) -> оксид міді (II) + вода.
Вкажіть тип реакції.
Що показує рівняння наступної хімічної реакції:
Яка кількість водню взаємодіє з 1 моль оксиду заліза (III)? Який об'єм водню взаємодіє з 1 моль оксиду заліза (III)? Яка кількість заліза при цьому утворюється? Скільки молекул води при цьому виходить?
Якщо у вас є виправлення або пропозиції до даного уроку, напишіть нам.
Якщо ви хочете побачити інші коригування та побажання до уроків, дивіться тут - Освітній форум.