Е211 Бензоат натрію, консервант, харчові добавки
Е 211 - бензоат натрію, відхаркувальний засіб, консервант харчових продуктів у виробництві повидла, мармеладу, меланжу, кільки, кетової ікри, плодово-ягідних соків, напівфабрикатів. Бензойну кислоту (Е 210), бензоат натрію (Е 211) і бензоат калію (Е 212) вводять в деякі харчові продукти як бактерицидний і протигрибковий засоби (джеми, фруктові соки, маринади і фруктові йогурти). Харчові добавки Е210 і Е211 можуть привести до злоякісних пухлин. Справа в тому, що при з'єднанні з вітаміном С утворюється бензол, який ушкоджує клітини нашого організму і може викликати онкологію.
Продукти, що містять бензоати натрію і кальцію, не рекомендується вживати астматикам і людям, чутливим до аспірину.
Вуглекислий газ є одним з основних компонентів газованих напоїв. Саме йому вони зобов'язані своєю назвою. Сам по собі він не небезпечний, але тим. хто страждає захворюваннями шлунково-кишкового тракту треба бути обережними, адже вуглекислий газ може спровокувати розлад травлення або больовий напад. При з'єднанні цього газу з водою утворюється вугільна кислота, що дратує слизову шлунка і кишечника. Ця кислота дуже нестійка і розкладається з утворенням вихідних продуктів: води і вуглекислого газу, викликаючи скупчення останнього в кишечнику.
Бензойна кислота і її солі Е 210-213. Безбарвні кристалічні речовини, кислота розчиняється в воді обмежено, солі добре. Входить до складу багатьох плодів і є поширеним природним консервантом. Бензойна кислота застосовується при виготовленні плодово-ягідних виробів, бензоати - при виробництві рибних консервів, маргарину, напоїв. ДСД становить 5 мг / кг маси тіла людини. Антимікробну дію кислоти пов'язано з її здатністю пригнічувати ферменти, які здійснюють окислювально-відновні реакції, і направлено, головним чином проти дріжджів і пліснявих грибів, включаючи афлатоксінобразующіе. Присутність білків в харчових системах послаблює активність бензойної кислоти, а фосфатів і хлоридів - підсилює. Бензойна кислота найбільш ефективна в кислому середовищі (рН менше 5), при цьому бензоати перетворюються в вільну кислоту. У нейтральних і лужних розчинах дію бензойної кислоти майже не відчувається. Для полегшення введення бензойної кислоти в рідкі харчові продукти використовують її солі - бензоати так як вони краще розчинні у воді.
Бензойна кислота Бензоат натрію
Дослідження бензойної кислоти
Матеріали для роботи:
- бензойна кислота (Е210) або натрію бензоат (Е211);
- 5% розчин водню пероксиду (свіжоприготованого);
- мідь сірчанокисла 5-водна, розчин з масовою концентрацією 5 г в 1 дм3 20% розчину оцтової кислоти;
- калію гідроокис, розчин масовою концентрацією 56 і 5,6 г / дм 3;
- сіль кухонна, розчин масовою концентрацією 250 г / дм 3;
- гидроксиламина гідрохлорид, розчин масовою концентрацією 200 г / дм 3;
- 0,1 н розчин гідроксиду натрію;
- кислота сірчана, розчин масовою концентрацією 49 г / дм 3;
- магній сірчанокислий 7-водний;
- спирт етиловий;
- 1% розчин фенолфталеїну;
- вода дистильована;
- піпетки на 1, 2, 10 см 3;
- бюретки;
- конічні колби на 100 мл;
- циліндр на 25 см 3.
Бензойна кислота (Е210) - С6 Н5 СООН - безбарвна кристалічна речовина зі слабким специфічним запахом, важко розчинна воді і добре в етиловому спирті і рослинних оліях. У 100 г води при кімнатній температурі розчиняється 0,34 г бензойної кислоти, а в 100 г масел - 1-2 м
Отримують в промисловості за технологічним регламентом окисленням толуолу. Термін зберігання 2 роки.
Органолептичні показники бензойної кислоти представлені в табл. 6
Органолептичні показники бензойної кислоти
Методи випробувань бензойної кислоти
Визначення масової частки бензойної кислоти
Метод заснований на нейтралізації бензойної кислоти 0,1 н розчином гідроксиду натрію в присутності 1% розчину фенолфталеїну.
Наважку бензойної кислоти в кількості 0,4 г поміщають в конічну колбу, розчиняють в 20 см 3 спирту, додають 2-3 краплі 1% розчину фенолфталеїну і титрують з бюретки 0,1 н розчином гідроксиду натрію до появи рожевого забарвлення розчину.
Масову частку бензойної кислоти (Х) в% обчислюють за фо рмуле:
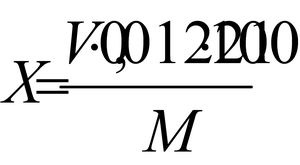
.
де V - об'єм 0,1 н розчину гідроксиду натрію, витрачений на титрування, см 3;
M - маса наважки, г;
0,01221 - маса бензойної кислоти, що відповідає 1 см 3 0,1 н розчину гідроксиду натрію.
Визначення бензойної кислоти в харчових продуктах
Метод заснований на отгонке бензойної кислоти з продукту водяною парою, взаємодії її з гідрохлоридом гідрооксіламіна і пероксидом водню в присутності іонів Сu ++ з утворенням забарвленого о-нитрозо-фенольного похідного, інтенсивність забарвлення якого вимірюють фотометричним. Межа виявлення бензойної кислоти - 0,005%.
Приготування основного розчину бензойної кислоти (100 мг / дм 3). Наважку бензойної кислоти 0,1 г вносять в мірну колбу на 1000 см 3 і додають розчин гідроксиду калію масової концентрації 5,6 г / см 3 до мітки.
Побудова градуювального графіка. Готують шість робочих розчинів. Для цього в сім конічних колб вносять піпеткою 0; 1,0; 2,0; 4,0; 6,0; 8,0 і 10,0 см 3 основного розчину бензойної кислоти. У кожну колбу додають 2,0 см 3 розчину гідроокису калію масової концентрації 56 г / дм 3 і доводять об'єм розчину в кожній колбі до 20 см 3. додаючи відповідно 18,0; 17,0; 16,0; 14,0; 12,0; 10,0 і 8,0 см 3 води. Отримані розчини містять 0; 0,1; 0,2; 0,4; 0,6; 0,8 і 1,0 мг бензойної кислоти
Готують розчин порівняння. Для цього в використовуваний робочий розчин вносять піпеткою по 2,0 см 3 розчину сірчанокислої міді, розчину гідрохлориду гідроксиламіну і розчину пероксиду водню, перемішують і вносять в кювету вимірювального приладу. Фотометрирование здійснюють через (15 ± 3) хвилин від моменту внесення реактивів, при світофільтрі 315 нм. Контрольним розчином служить розчин порівняння, що не містить бензойної кислоти.
За отриманими даними будують градуйований графік в системі коор рдінат: оптична щільність - маса бензойної кислоти в розчині.
Хід визначення. У посудину для перегонки (рис. 1) поміщають навішення продукту масою від 5 до 10 г або 5-10 см 3 рідкого продукту, додають 10,0 см 3 розчину сірчаної кислоти і 10 г сірчанокислого магнію.
У мірну колбу-приймач вливають 10,0 см 3 розчину гідроокису калію масової концентрації 56 г / дм 3.
Отгонную колбу наповнюють на 3/4 об'єму розчином хлористого н атрія і починають нагрівати при відкритому крані.
Через кілька хвилин після закипання рідини в отгонной колбі кран закривають і починають отгонку, регулюючи нагрівання колби так, щоб обсяг рідини в посудині для перегонки був постійним і рівним приблизно 20 см 3. Перегонку закінчують після отримання 100 см 3 відгону в приймальні колбі.
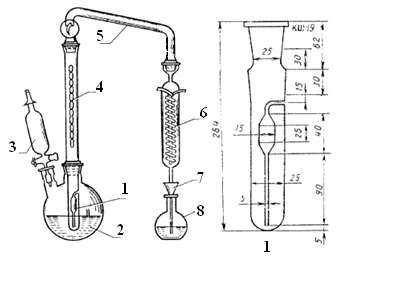
Мал. 1. Установка для перегонки:
1 - посудина для перегонки; 2 - двугорлая колба; 3 - делительная воронка з кр Аном; 4 - дефлегматор;
5 - каплеул овітель; 6 - холодильник; 7 - скляна воронка; 8 - мірна колба
За 20 см 3 відгону вносять піпеткою в дві конічні колби. Потім в відгін додають піпеткою по 2 см 3 розчинів сірчанокислої міді, гідрохлориду гідроксиламіну і пероксиду водню, витримують і фотометрируют.
В якості контрольного використовують розчин з додаванням усіх реактив ІВВВ для отримання забарвленого похідного.
За отриманого значення оптичної щільності за допомогою градуювального графіка знаходять масу бензойної кислоти в досліджуваному розчин оре.
Обробка результатів. Масову частку бензойної кислоти (Х) у відсотках обчислюють за формулою:
Приготування водних розчинів. На практиці найчастіше використовують водні розчини сорбата калію, бензоату натрію або їх сумішей (зазвичай в співвідношенні 1: 1) з концентрацією від 5 до 25%. Розчини сорбата можна готувати більш високої концентрації (до 40%). Для приготування розчину потрібну кількість консерванту розчиняють приблизно в половині необхідного обсягу питної води, нагрітої до температури 50. 80 ° С. Після повного розчинення солі в отриманий розчин додають воду, що залишилася і ретельно перемішують. Рекомендується відфільтрувати розчин через шар бавовняної тканини (бязі).
Якщо консервант розчинений в жорсткій воді, то розчин може бути злегка мутним, але це не впливає на його консервативну дію. До розчинів не слід додавати лимонну і інші кислоти, так як це може призвести до випадання осаду малорозчинних у воді сорбінової або бензойної кислот.
Розчини консервантів мають обмежений термін зберігання. В ідеалі вони повинні бути свіжоприготовленими.
У книзі представлені дані про роль і місце біологічно активних харчових добавок (БАПД) при активних заняттях спортом.

Розглянуто характеристика застосовуваних в даний час харчових інгредієнтів (харчові добавки, ароматизатори, технологічні допоміжні засоби) і біологічно активних добавок.

Словник харчових добавок складається з словникових статей по єдиній структурі, описаної на початку книги, і розташованих в порядку зростання Е-індексів. Словникові статті про добавках, яким не присвоєно Е-індекси, винесені в кінець словника і розташовані в алфавітному порядку.

Описано широко застосовуються в самих різних галузях харчової промисловості стабілізатори, загусники і гелеутворювачі. Розглянуто майже всі відомі в даний час речовини цієї групи, наведені їх хімічні формули і властивості, вказані джерела і способи отримання. Книга призначена для фахівців харчової промисловості, а також буде корисна студентам і аспірантам профільних вищих навчальних закладів.

Інділайт Стейк з грудки, охолоджений, 700 г

Інділайт Котлета натуральна, охолоджена, 700 г

Інділайт Кульки з індички, охолоджені, 450 г
Шановні клієнти! Звертаємо вашу увагу на те, що упаковка може мати кілька видів.

Інділайт Печінка індички, охолоджена, 700 г

Інділайт Котлети з м'яким сиром і цибулею пореєм, охолоджені, 450 г

Інділайт Котлети з індички з паприкою, охолоджені, 450 г

Інділайт Шніцель "Апетитний" з індички, охолоджений, 450г

Інділайт Купати "По-домашньому" з індички, охолоджені, 500 г

Інділайт Гуляш з індички, охолоджений, 700 г